min
Sekce:
Denní přehled
Notifikační e-maily z ISZP
SÚKL informuje o notifikačních emailehc upozorňujících na konec platnosti činnosti v ISZP.
SÚKL
05. 02. 2025
min
Sekce:
Denní přehled
Aktualizace pokynů SÚKL
SÚKL aktualizoval pokyny týkající se správních poplatků a náhrad výdajů za odborné úkony.
SÚKL
27. 01. 2025
min
Sekce:
Denní přehled
SÚKL informuje o PMFC zkouškách u zdravotnických prostředků
SÚKL upozorňuje na oznamovací povinnost zadavatelů provádějících PMCF zkoušku, která zahrnuje vystavení subjektů jiným postupům, než jaké se provádějí za běžných podmínek použití prostředku.
SÚKL
17. 01. 2025
min
Sekce:
Denní přehled
Aktualizace pokynu CAU-13
SÚKL aktualizoval pokyn týkající se postupu klinického hodnocení léčivých přípravků/PZLÚ pro účely úhradové regulace.
SÚKL
16. 01. 2025
min
Sekce:
Denní přehled
Upozornění pro výrobce zdravotnických prostředků
SÚKL zveřejnil upozornění na účinnost části Nařízení Evropského parlamentu a Rady (EU) 2024/1860, které ukládají výrobcům prostředků hlásit informace o přerušení nebo ukončení výroby prostředků.
SÚKL
10. 01. 2025
min
Sekce:
Denní přehled
Hloubková revize v roce 2025
SÚKL zveřejnil orientační přehled skupin v zásadě terapeuticky zaměnitelných léčivých přípravků, u kterých zahájí hloubkovou revizi systému úhrad v 1. polovině roku 2025.
SÚKL
08. 01. 2025
min
Sekce:
Vizualizace dat
Rozhodnutí SÚKL a MZ ČR v oblasti cen a úhrad
Od 1. 1. 2025 nabízí společnost Pharmeca a.s. na svých stránkách přehled vydaných rozhodnutí SÚKL a MZ ČR v oblasti cen a úhrad.
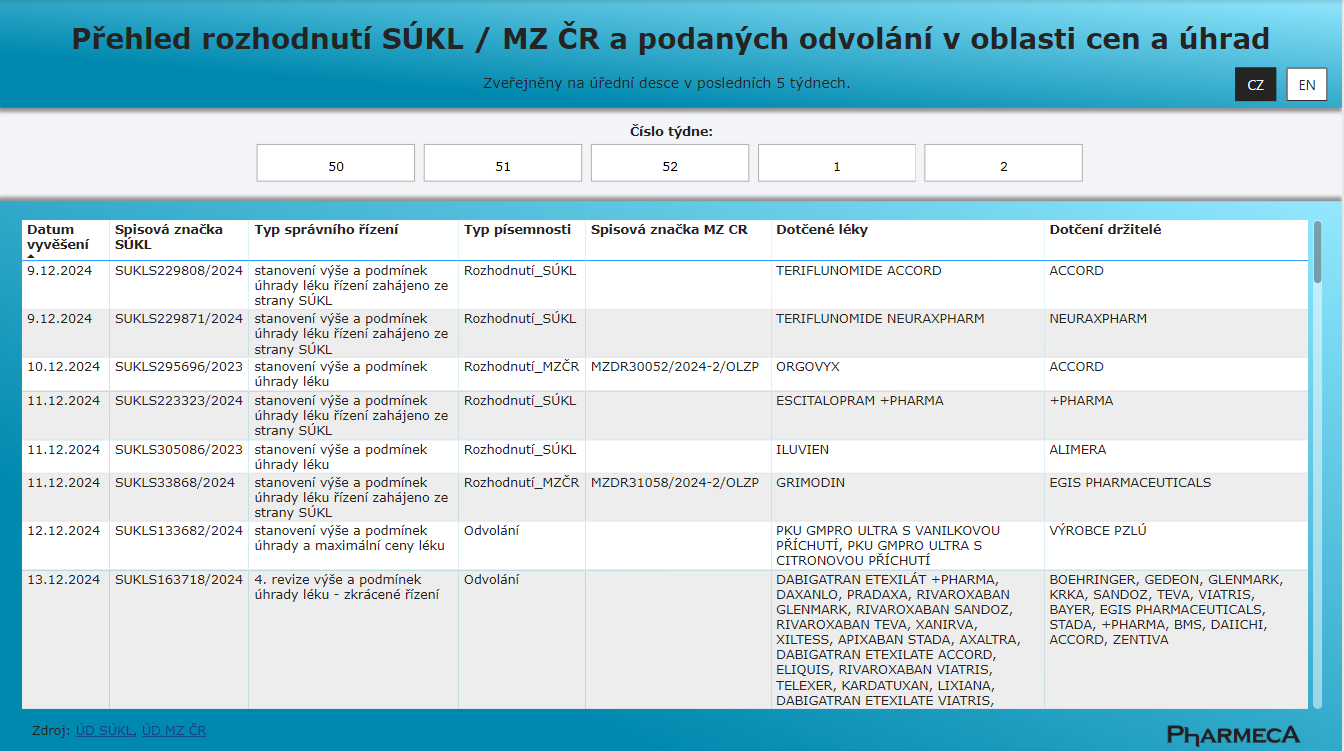

Pharmeca a.s.
08. 01. 2025
min
Sekce:
Denní přehled
Vyjádření MZ ČR k otázce distribuce do zahraničí
Pharmeca a. s. upozorňuje výrobce, držitele rozhodnutí o registraci a distributory na vyjádření Ministerstva zdravotnictví ČR k otázce zákazu distribuce do zahraničí.
MZ ČR
06. 01. 2025

