Sekce:
Zaměřeno na
Říjen je měsíc AI
Víte, co je AI Act a jak se projeví v praxi?
Pharmeca a.s.
01. 10. 2024
Sekce:
Denní přehled
Proč se bojíme zásilkového výdeje léčiv?
Dne 26. 6. 2024 se uskuteční kulatý stůl na téma Proč se bojíme zásilkového výdeje léčiv.
PSP ČR
20. 06. 2024
Sekce:
Denní přehled
Léčivé přípravky
Dne 21. 6. 2024 se uskuteční odborná konference na téma Léčivé přípravky.
PSP ČR
17. 06. 2024
Sekce:
Zaměřeno na
Informační systém klinických studií (CTIS) - současnost a budoucnost
CTIS podporuje interakce mezi sponzory klinických studií (výzkumníky nebo společnostmi, které provádějí klinickou studii a shromažďují a analyzují data) a regulačními orgány v členských státech EU...
Pharmeca
08. 03. 2024
Sekce:
Zaměřeno na
Změna sazby DPH na léčiva
Na základě změny zákona č. 235/2004 Sb., o dani z přidané hodnoty, došlo od 1. 1. 2024 ke změně sazeb DPH, což mělo dopad zejména na zvýšení cen a úhrad léčivých přípravků. V infografice si...
Pharmeca a.s.
27. 02. 2024
Sekce:
Vizualizace dat
Kurzy pro cenovou referenci na klik
Základní informací pro provedení cenové reference v řízení o stanovení cen a úhrad léků je průměrný směnný kurz v předchozím čtvrtletí. Nově si přehled všech potřebných směnných kurzů můžete najít...
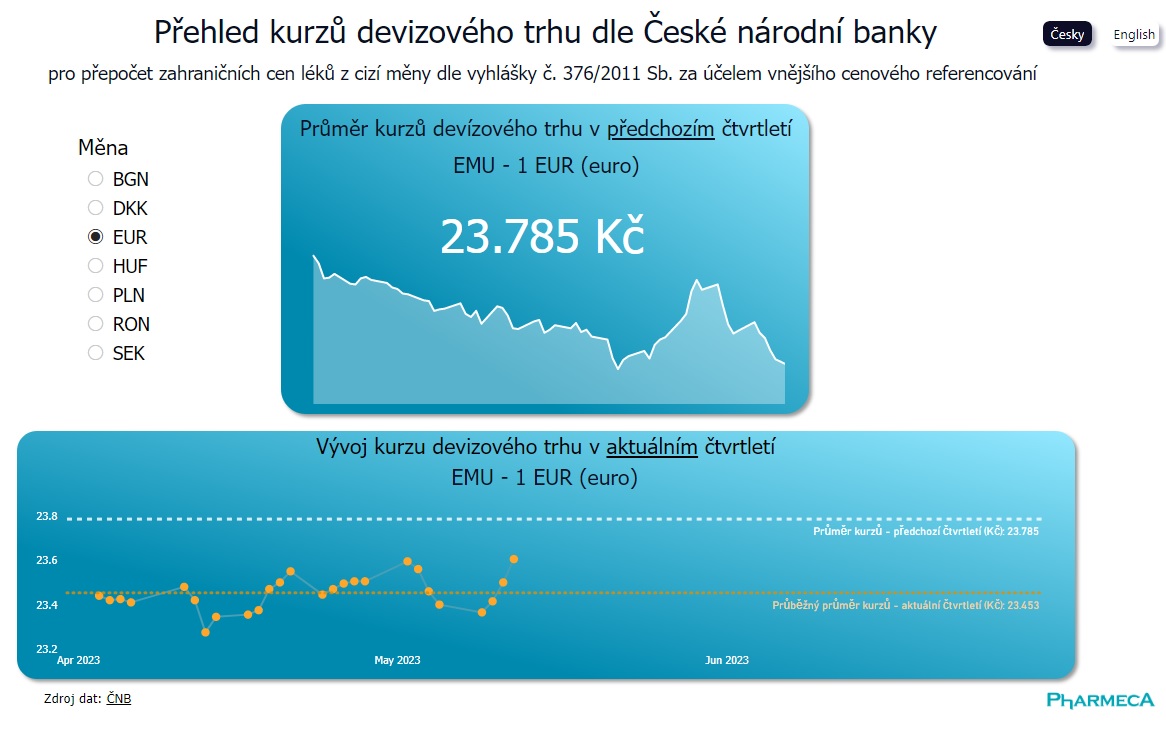

Pharmeca a.s.
15. 05. 2023
Sekce:
Zaměřeno na
Cesta léku
Objevením účinné látky začíná dlouhý proces ověřování vhodnosti a bezpečnosti léku před jeho uvedením na trh. Proces sledování u léků však nekončí ani úspěšnou registrací.
Pharmeca a.s.
17. 04. 2023
Sekce:
Zaměřeno na
Novela zákona o léčivech v boji proti nedostupnosti léků v ČR
Dne 24. 3. 2023 bylo ukončeno připomínkové řízení k novele zákona o léčivech, která by měla pomoci řešit nedostupnost léků v ČR.
Pharmeca a.s.
29. 03. 2023

